Nature:新研究鉴定出调节神经干细胞衰老的基因
来源:生物谷原创 2024-10-22 11:27
在一项新的研究中,来自斯坦福大学医学院的研究人员揭示了作为成体大脑中生成新神经元的细胞群体,神经干细胞如何以及为何随着年龄的增长而变得不那么活跃。
人类大脑中的大多数神经元都会终生存在,这是有充分理由的。神经元突触之间复杂的结构关系中保存着错综复杂的长期信息。失去神经元就等于失去了这些关键信息,也就是遗忘。
耐人寻味的是,在成体大脑中,一些新的神经元仍然由一个叫做神经干细胞的细胞群体产生。然而,随着年龄的增长,大脑越来越不善于制造这些新的神经元,这种趋势可能会对神经系统造成破坏性后果,不仅影响记忆力,还会影响阿尔茨海默病和帕金森病等退化性脑部疾病,以及中风或其他脑损伤后的恢复。

在一项新的研究中,来自斯坦福大学医学院的研究人员揭示了作为成体大脑中生成新神经元的细胞群体,神经干细胞如何以及为何随着年龄的增长而变得不那么活跃。相关研究结果于2024年10月2日在线发表在Nature期刊上,论文标题为“CRISPR–Cas9 screens reveal regulators of ageing in neural stem cells”。
这项研究还提出了一些有趣的后续步骤,通过靶向新发现的可以重新激活神经干细胞的途径,来解决年老的神经干细胞的钝态,甚至刺激需要修复的年轻大脑中的神经发生,即新神经元的产生。
斯坦福大学医学院遗传学教授Anne Brunet博士和她的团队利用CRISPR平台(一种允许科学家精确编辑活细胞遗传密码的分子工具),在全基因组范围内寻找基因,当敲除这些基因时,可以提高来自老龄小鼠的体外培养样本中神经干细胞的激活,但不能提高来自年轻小鼠的体外培养样本中神经干细胞的激活。
Brunet强调说,“我们首先发现了300个具有这种能力的基因,这已经很多了。”在将候选基因缩小到 10 个之后,“有一个基因特别引起了我们的注意”,Brunet说,“它是称为GLUT4蛋白的葡萄糖转运体的编码基因,这表明年老神经干细胞内和周围的葡萄糖水平升高可能使这些细胞处于不活跃状态”。
动态的大脑
Brunet实验室博士后学者Tyson Ruetz博士说,在大脑的某些部位,如海马体和嗅球,许多神经元的寿命较短,它们会定期过期,并可能被新的神经元取代。他说,“在大脑中这些更具活力的部分,至少在年轻健康的大脑中是这样,新的神经元不断诞生,短暂存在的神经元被新的神经元取代。”
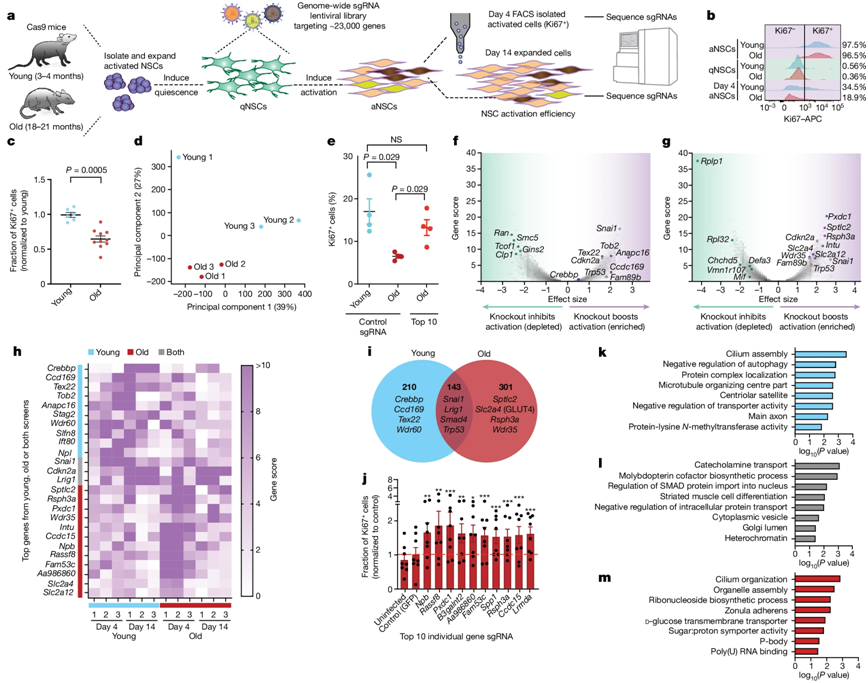
图片来自Nature, 2024, doi:10.1038/s41586-024-07972-2
Brunet说,Ruetz开发了一种在体内测试新发现的遗传通路的方法。Ruetz利用了大脑中神经干细胞被激活的部位——室管膜下区(subventricular zone),与新的神经元增殖和迁移到的地方——嗅球之间的距离。在小鼠大脑中,嗅球与室管膜下区相距数毫米。
通过敲除室管膜下区中的GLUT4基因,等待数周,然后计算嗅球中新神经元的数量,他们证实敲除该基因确实对神经干细胞有激活和增殖作用,导致活的小鼠体内新神经元的产生显著增加。通过最高干预,他们观察到年老小鼠的新生神经元增加了两倍以上。
Ruetz说,“这让我们能够观察到神经干细胞的三个关键功能。首先,我们可以看出它们正在增殖。第二,我们可以看到它们正在向嗅球迁移,它们应该在那里。第三,我们可以看到它们正在该部位形成新的神经元。”
Ruetz说,同样的技术也可能应用于大脑损伤研究。“室管膜下区中的神经干细胞也在修复中风或脑外伤造成的脑组织损伤。”
一个充满希望的发现
Brunet说,这种GLUT4关联性“是一个充满希望的发现”。首先,它不仅表明有可能设计出药物或基因疗法,以开启年老或受伤大脑中新神经元的生长,还表明有可能开发出更简单的行为干预措施,如低碳水化合物饮食,从而调整年老神经干细胞吸收的葡萄糖数量。
Brunet团队还发现了其他值得后续研究的途径。与初级纤毛有关的基因也与神经干细胞的激活有关。初级纤毛是一些脑细胞的组成部分,在感知和处理生长因子和神经递质等信号方面发挥着关键作用。
这一发现让Brunet团队确信他们的方法是有效的,部分原因是之前无关的研究工作已经发现了纤毛分布与神经干细胞功能之间的关联。Brunet说,这也很令人兴奋,因为与葡萄糖传递的新线索的联系可能指向潜在同时涉及这两种途径的替代治疗途径。她说,“初级纤毛,它们影响干细胞静止、代谢和功能的能力,与我们发现的葡萄糖代谢之间可能存在有趣的交谈。”
Brunet接续说,“下一步,我们将更仔细地研究葡萄糖限制,而不是敲除葡萄糖转运基因,在活体动物中的作用。”(生物谷Bioon.com)
参考资料:
Tyson J. Ruetz et al. CRISPR–Cas9 screens reveal regulators of ageing in neural stem cells. Nature, 2024, doi:10.1038/s41586-024-07972-2.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


